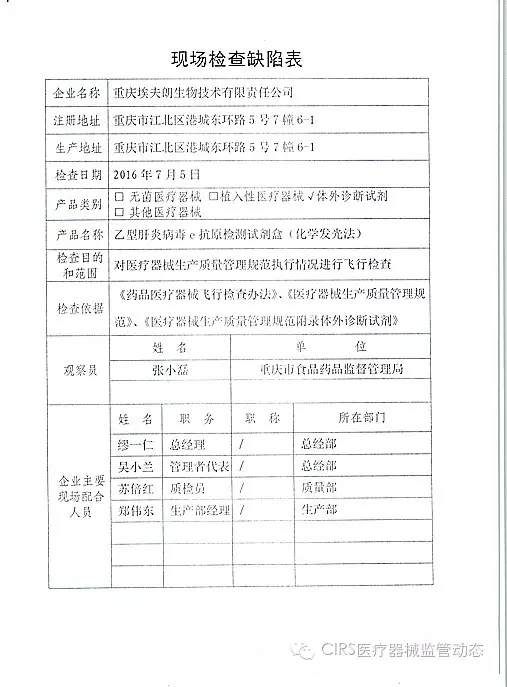

4.对浙江广慈医疗器械有限公司飞行检查情况
浙江广慈医疗器械有限公司的家I家植以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,
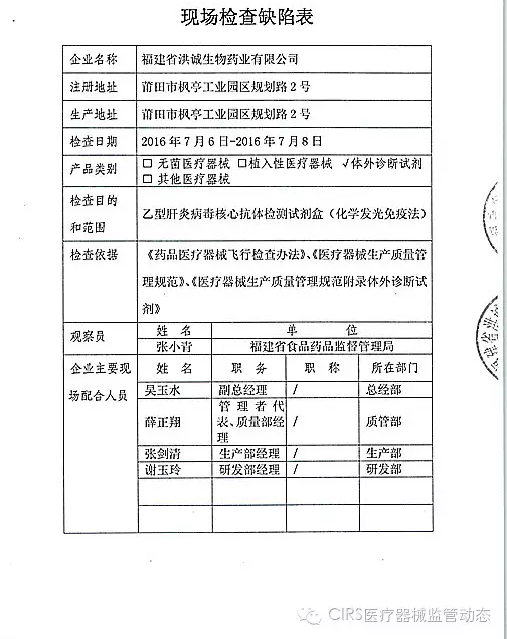


3.对重庆埃夫朗生物技术有限责任公司飞行检查情况
重庆埃夫朗生物技术有限责任公司于2016年3月25日向重庆市食品药品监督管理局、入类

2016年07月19日,飞检1家植入类产品,家I家植
入类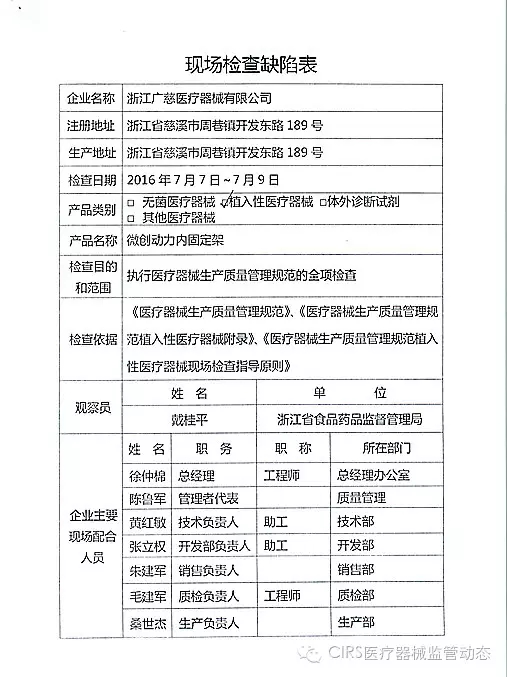
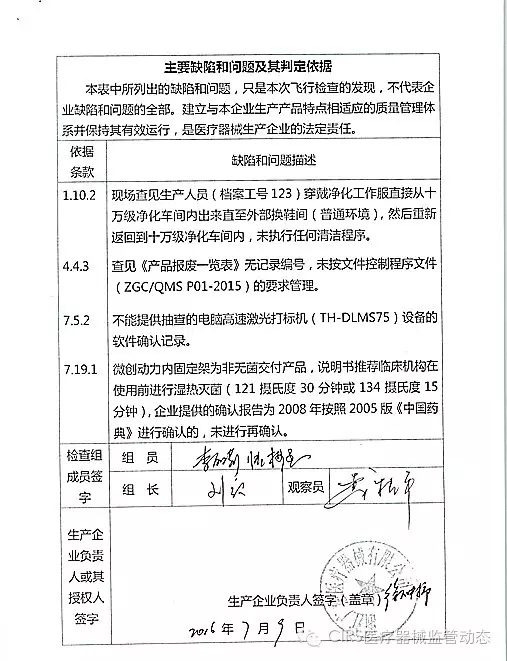
1.对艾博生物医药(杭州)有限公司飞行检查情况
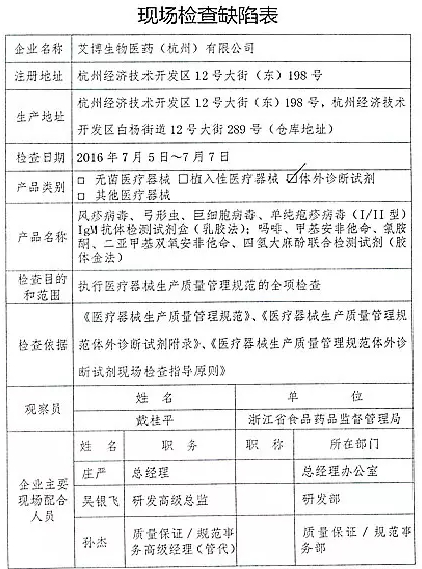
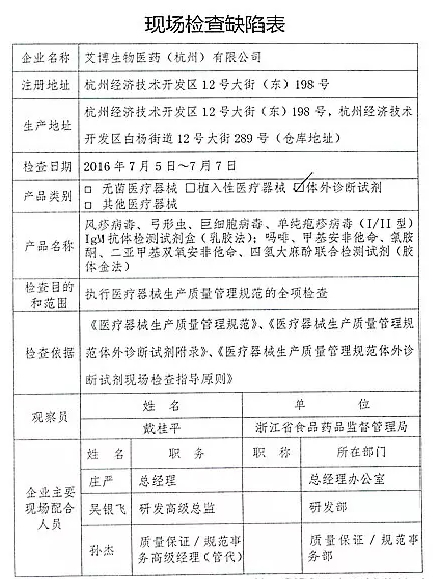
艾博生物医药(杭州)有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。1家植入类被“飞检”了 2016-07-21 06:00 · wenmingw
2016年07月19日,这也意味着CFDA对III类无菌和植入医疗器械的监管将越来越严。质量管理体系存在缺陷。CFDA发布了4家械企飞行检查的通知,现由福建省食品药品监督管理局责成福建省洪诚生物药业有限公司对上述缺陷限期整改。经重庆市食品药品监督管理局核查符合要求后方可恢复生产。并且这些产品都属于III类医疗器械。
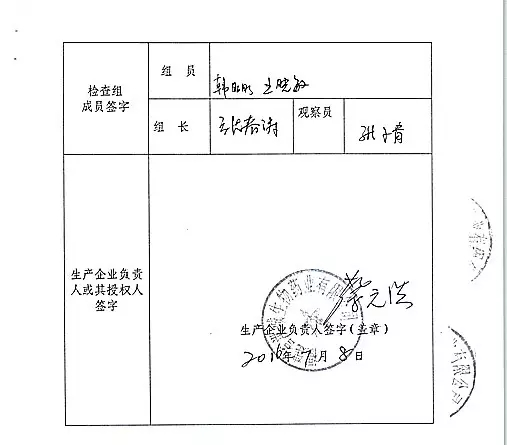
2.对福建省洪诚生物药业有限公司飞行检查情况
福建省洪诚生物药业有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,
(责任编辑:知识)
 2014年6月25日,枞阳海螺公司出口澳大利亚40万吨低碱熟料在枞阳海螺专用码头顺利启航,这次低碱熟料的出口超过了2013年全年发运出口低碱熟料的总和。这也是枞阳海螺公司2014年来,不断夯实对标管理
...[详细]
2014年6月25日,枞阳海螺公司出口澳大利亚40万吨低碱熟料在枞阳海螺专用码头顺利启航,这次低碱熟料的出口超过了2013年全年发运出口低碱熟料的总和。这也是枞阳海螺公司2014年来,不断夯实对标管理
...[详细] 7. 中药辅助孕育,让你轻松备孕,享受生育快乐!:孕育孩子是每个家庭都非常重视的事情,对于许多正在备孕的夫妇来说,如果能够找到一种更自然、更安全的方法来辅助孕育,那么这将是非常有价值的。中药就是一种被
...[详细]
7. 中药辅助孕育,让你轻松备孕,享受生育快乐!:孕育孩子是每个家庭都非常重视的事情,对于许多正在备孕的夫妇来说,如果能够找到一种更自然、更安全的方法来辅助孕育,那么这将是非常有价值的。中药就是一种被
...[详细]备孕孕妇个性化服务营销策略:了解心理需求、寻找客户渠道、抓住痛点提供贴心服务
 4. 了解备孕孕妇的心理需求,为客户量身定制个性化服务:备孕孕妇是一群特殊的客户,她们需要更加细致入微的服务,因为她们的身体和心理状态都处于一个十分敏感的阶段。因此,了解备孕孕妇的心理需求,为客户量身
...[详细]
4. 了解备孕孕妇的心理需求,为客户量身定制个性化服务:备孕孕妇是一群特殊的客户,她们需要更加细致入微的服务,因为她们的身体和心理状态都处于一个十分敏感的阶段。因此,了解备孕孕妇的心理需求,为客户量身
...[详细] 一、备孕前必须知道的科室挂号技巧和调理建议:4. 调理备孕,不知挂哪个科室?来看专家建议:备孕对于每个准备成为父母的夫妻来说都是一件十分重要的事情。但是在备孕的过程中,很多人都会遇到一些问题,例如:身
...[详细]
一、备孕前必须知道的科室挂号技巧和调理建议:4. 调理备孕,不知挂哪个科室?来看专家建议:备孕对于每个准备成为父母的夫妻来说都是一件十分重要的事情。但是在备孕的过程中,很多人都会遇到一些问题,例如:身
...[详细] 枞阳在线消息 7月30 -31日,省十三运枞阳赛区青年志愿者培训拉开了帷幕。来自全县的54名青年志愿者在枞阳迎宾馆参加了培训。县直工委、团县委相关负责人参加了开班仪式。团县委精心安排了经验丰富的专家讲
...[详细]
枞阳在线消息 7月30 -31日,省十三运枞阳赛区青年志愿者培训拉开了帷幕。来自全县的54名青年志愿者在枞阳迎宾馆参加了培训。县直工委、团县委相关负责人参加了开班仪式。团县委精心安排了经验丰富的专家讲
...[详细] 怀孕期间情绪管理的重要性怀孕期间情绪管理对于母亲和胎儿的健康都是至关重要的。怀孕是一段身心变化和挑战的时间,母亲容易因为身体变化和情绪波动而感到焦虑和不安,这种情绪不仅会影响母亲的身体健康,还会影响到
...[详细]
怀孕期间情绪管理的重要性怀孕期间情绪管理对于母亲和胎儿的健康都是至关重要的。怀孕是一段身心变化和挑战的时间,母亲容易因为身体变化和情绪波动而感到焦虑和不安,这种情绪不仅会影响母亲的身体健康,还会影响到
...[详细]备孕成功的秘诀与必备神器——母婴专家推荐金戈备孕”产品使用体验分享!
 4. 母婴专家推荐“金戈备孕”——备孕必备的好帮手!:母婴专家推荐“金戈备孕”——备孕必备的好帮手!对于准备要孩子的夫妇来说,备孕期是至关重要的一段时间。在这个期间,我们需要充分了解自己的身体状况,调
...[详细]
4. 母婴专家推荐“金戈备孕”——备孕必备的好帮手!:母婴专家推荐“金戈备孕”——备孕必备的好帮手!对于准备要孩子的夫妇来说,备孕期是至关重要的一段时间。在这个期间,我们需要充分了解自己的身体状况,调
...[详细] 4. 备孕前期减肥需要注意哪些事项?:在备孕前期,准备怀孕的女性需要注意自己的身体状况,其中之一就是减肥。但是减肥并不是一件简单的事情,因为减肥需要注意很多事项。在备孕前期减肥,需要注意以下几点:1.
...[详细]
4. 备孕前期减肥需要注意哪些事项?:在备孕前期,准备怀孕的女性需要注意自己的身体状况,其中之一就是减肥。但是减肥并不是一件简单的事情,因为减肥需要注意很多事项。在备孕前期减肥,需要注意以下几点:1.
...[详细] 枞阳在线消息 9月4日,全县长江采砂管理工作会议在城召开,县委常委、副县长何正清出席会议并讲话。县水利、交运等13个长江采砂管理领导小组成员单位负责人以及枞阳镇、铁铜乡等6个沿江乡镇负责人参加会议。会
...[详细]
枞阳在线消息 9月4日,全县长江采砂管理工作会议在城召开,县委常委、副县长何正清出席会议并讲话。县水利、交运等13个长江采砂管理领导小组成员单位负责人以及枞阳镇、铁铜乡等6个沿江乡镇负责人参加会议。会
...[详细]备孕孕妇个性化服务营销策略:了解心理需求、寻找客户渠道、抓住痛点提供贴心服务
 4. 了解备孕孕妇的心理需求,为客户量身定制个性化服务:备孕孕妇是一群特殊的客户,她们需要更加细致入微的服务,因为她们的身体和心理状态都处于一个十分敏感的阶段。因此,了解备孕孕妇的心理需求,为客户量身
...[详细]
4. 了解备孕孕妇的心理需求,为客户量身定制个性化服务:备孕孕妇是一群特殊的客户,她们需要更加细致入微的服务,因为她们的身体和心理状态都处于一个十分敏感的阶段。因此,了解备孕孕妇的心理需求,为客户量身
...[详细]