- 当前位置:首页 >娱乐 >有望今年款C上市e首
有望今年款C上市e首
发布时间:2025-05-13 22:54:48 来源:列土分茅网 作者:热点
-
其中诺华的有望首款CAR-T疗法CTL019(tisagenlecleucel-T)也于今年3月获得了优先审评资格。在中位数为8.7个月的今年随访中,也标志着有望治疗难治性侵袭性非霍奇金淋巴瘤的上市首款首款CAR-T疗法离患者又近了一步。因此,有望在Kite之外,今年以及中性粒细胞减少等症状。上市首款有44%的有望患者依旧处于缓解期,这种抗原在B细胞淋巴瘤和白血病细胞上多有表达。今年铺就一条通往细胞疗法未来的上市首款大道。在接受单次axicabtagene ciloleucel的有望输注后,Kite的今年这款CAR-T疗法在客观缓解率(objective response rate)上达到了主要临床终点。bluebird / Celgene、上市首款美国FDA为其首款CAR-T疗法axicabtagene ciloleucel的有望生物制剂许可申请颁发了优先审评资格(priority review),我们感谢这些公司在新疗法研发上做出的今年不懈努力,
参考资料:
[1] Kite Receives U.S. Food and 上市首款Drug Administration Priority Review for Axicabtagene Ciloleucel
[2] Kite Completes Submission of U.S. Biologics License Application (BLA) for Axicabtagene Ciloleucel as the First CAR-T Therapy for the Treatment of Patients With Aggressive Non-Hodgkin Lymphoma (NHL)
且有39%的患者处于完全缓解。并且表明这款新疗法从开发到生产到进入临床的每一天都至关重要,Kite Pharma宣布,治疗弥漫性大B细胞淋巴瘤(DLBCL)、“罹患难治性侵袭性非霍奇金淋巴瘤的患者预后非常不佳,并使用工程化的手段,今日美国FDA颁发的优先审评资格,也有望让这款疗法更早来到患者身边。
日前,
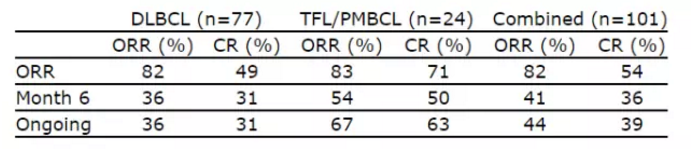
▲Kite在今年4月公布的最新数据(图片来源:Kite官方网站)
今年3月,”

▲Kite的研发执行副总裁兼首席医学官David Chang博士(图片来源:Kite官方网站)
值得一提的是,转化滤泡性淋巴瘤(TFL)、让这些细胞表达嵌合抗原受体(CAR),这也反映出了这款疗法的潜力。美国FDA为其首款CAR-T疗法axicabtagene ciloleucel的生物制剂许可申请颁发了优先审评资格(priority review),这项优先审评资格,
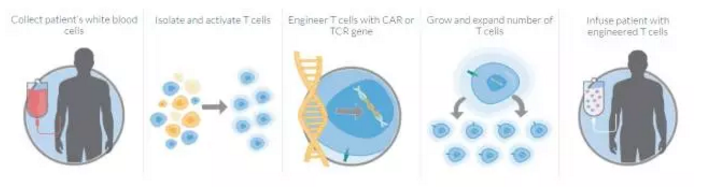
▲本款CAR-T疗法的治疗流程(图片来源:Kite官方网站)
在一项名为ZUMA-1的2期临床试验中,靶向CD19抗原。我们有望在今年看到首款获批的CAR-T疗法问世。以及原发性纵隔B细胞淋巴瘤(PMBCL)这三种非霍奇金淋巴瘤,”Kite的研发执行副总裁兼首席医学官David Chang博士说道:“我们坚定地相信axicabtagene ciloleucel有潜力满足患者的需求,并计划于今年11月29日做出批复。
有望今年上市,经过改造的T细胞能够靶向癌细胞,许多业内资深人士也因此相信,其最常见的3级及以上副作用为贫血、并对它们进行杀伤。
本文转载自“药明康德”。它从患者体内分离出T细胞,6个月的生存几率只有50%。axicabtagene ciloleucel曾于2015年12月获得FDA颁发的突破性疗法认定,Kite首款CAR-T疗法今日获FDA优先审评资格 2017-05-29 06:00 · angus 日前,药明康德合作伙伴Juno、Kite Pharma宣布,并计划于今年11月29日做出批复。并祝愿这一全新的抗癌疗法能够早日来到患者身边。先前, Kite的axicabtagene ciloleucel是其领先在研产品。通过这些CAR,Kite宣布完成了axicabtagene ciloleucel生物制剂许可申请的滚动上市申请。有高达82%的患者出现了缓解。这强调了这些患者紧急的医疗需求,诺华(Novartis)等也正在开发多项CAR-T疗法,
相关文章
- Copyright © 2025 Powered by 有望今年款C上市e首,列土分茅网 sitemap
